
Innehåll
I den här artikeln: Förbereda proverna Realisera experimentet Analysera resultaten av absorbansen12 Referenser
Spektrofotometri är en experimentell metod som används för att mäta lösningens koncentration av en lösning genom att beräkna mängden ljus som absorberas av detta lösta ämne. Denna teknik är baserad på egenskaperna hos vissa kemiska föreningar för att absorbera olika våglängder av ljus med olika intensiteter. Du kan känna till ämnena i en lösning och deras koncentrationer bara genom att leda ljus genom den. För detta använder forskningslaboratorier en enhet som kallas en spektrofotometer.
stadier
Del 1 Förbered proverna
-

Slå på spektrofotometern. De flesta enheter måste stanna ett tag i drift innan de kan ge exakta mätningar. Starta maskinen och låt den värmas upp i minst 15 minuter innan du analyserar din första lösning.- Utnyttja den här tiden för att förbereda dina prov.
-

Rengör kyvetterna. Om du utför praktiskt arbete i en skolmiljö kan du förses med engångsrör som du inte behöver rengöra. Om du använder återanvändbara behållare, se till att de är helt rena innan du använder dem. Skölj noggrant med destillerat vatten.- Ta hand om skålarna, det är ganska dyrt material.
- När du hanterar en skål ska du inte lägga fingrarna på de sidor som ljuset passerar genom. I allmänhet är det dessa transparenta ansikten.
-

Häll rätt volym i skålen. Vissa kyvetter har en maximal kapacitet på 1 ml, medan provrören kan vara upp till 5 ml. För att din mätning ska vara relevant är det viktigt att uppmärksamma det faktum att laserstrålen som fungerar som en ljuskälla passerar genom vätskan och inte den tomma delen av behållaren.- Om du fyller dina prov med en pipett, ändra den varje gång för att undvika korskontaminering.
-

Förbered en "vit". Denna term avser kontrolllösningen som inte innehåller något annat än lösningsmedlet i vilket det lösta ämnet som ska analyseras kommer att lösas. Om du till exempel utför ditt experiment på saltvatten kommer din "vita" endast att bestå av vatten. Om du har tonat ditt saltvatten i rött, kommer den "vita" att innehålla vatten och rött färgämne. Denna kontrolllösning måste ha samma volym och placeras i samma behållare som lösningen som ska studeras. -
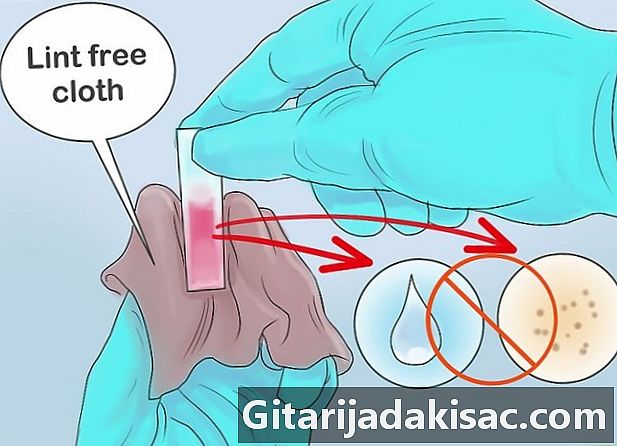
Torka av skålen. Innan du lägger den i spektrofotometern, kontrollera att den är så ren som möjligt för att förhindra att damm eller smuts snedvrider resultatet. Använd en luddfri trasa för att ta bort damm och torka eventuella droppar vatten som kan finnas på ytterväggarna.
Del 2 Förverkliga upplevelsen
-

Ställ in våglängden. Du väljer nu våglängden för ljuset som kommer att passera genom provet. Det måste bara finnas en våglängd (det betyder att färgen måste vara monokrom) för att resultatet ska bli tillförlitligt. Välj ett ljus vars färg du vet absorberas av en av de kemiska föreningarna i lösningen. Se Spectrophotometer användarhandbok för att avgöra vilken inställning som är mest relevant.- Om du gör praktiskt arbete i skolan kommer våglängden förmodligen att ges till dig.
- Den våglängd som valts för att utföra experimentet kommer alltid att skilja sig från provets färg. Du vet faktiskt redan att lösningen kommer att returnera allt ljus i våglängden som motsvarar dess synliga färg.
- Objekt har en färg för det mänskliga ögat eftersom de reflekterar vissa våglängder medan de absorberar andra. Till exempel är gräset grönt eftersom klorofylen ger tillbaka det gröna ljuset medan det absorberar de andra nyanserna.
-

Kalibrera maskinen med det vita. Placera kontrolllösningen i skålhållaren och stäng locket. Om du har en analog spektrofotometer ser du en ratt med en nål som svänger enligt den upptäckta ljusintensiteten. Normalt, när du analyserar det vita, bör denna nål peka till höger. Skriv ner det erhållna värdet, du kan behöva det senare. Innan du tar bort skålen, vrid tarraknappen till noll.- Principen för kalibrering av en elektronisk spektrofotometer är densamma, förutom att mätningarna läses på en skärm. Tara enheten så att den är noll med hjälp av knappen för detta ändamål.
- Maskinens kalibrering förblir i minnet efter att kontrolllösningen har tagits bort. När du sedan gör mätningar med dina prover subtraheras ämnets absorbans automatiskt.
-

Ta bort det vita. Kontrollera att nålen eller skärmen förblir noll. För att vara säker på att kalibreringen har registrerats korrekt, försök att sätta tillbaka kontrolllösningen i maskinen. Mätningen måste alltid förbli lika med noll.- Om maskinvredet visar ett annat resultat börjar du tar igen från början.
- Om detta inte löser problemet, be någon om hjälp eller få maskinen service.
-

Mät absorbansen av dina prover. Vänta cirka 10 sekunder tills nålen stabiliseras eller den digitala displayen inte längre varierar. Skriv ner värdet på absorbansen och / eller transmissionen.- Den del av ljus som överförs genom provet är omvänt proportionell mot den del av ljus som absorberas. I allmänhet noteras värdet på absorbansen, som normalt uttrycks i decimalform, istället. Exempelvis kan ett resultat av 0,43 erhållas.
- För varje prov, gör minst tre mätningar och genomsnitt sedan de tre resultaten. Detta är det bästa sättet att få en så exakt figur som möjligt.
-

Upprepa med olika färger. Det är inte uteslutet att ditt prov innehåller många okända kemiska föreningar vars absorbans varierar beroende på den valda våglängden. För att minska felmarginalen gör du om mätningar genom att välja färger från 25 nm på ljusspektrumet. Du kommer att kunna upptäcka parasitiska ämnen som kan vara i din lösning.
Del 3 Analysera absorbansresultat
-

Beräkna transmittansen och absorbansen. Överföringen representerar andelen ljus som har passerat genom provet och nått spektrofotometersensorn. Däremot kännetecknar absorbansen den del av ljus som har absorberats av en av de kemiska ämnena i lösningen. De flesta moderna enheter visar absorbans- och transmissionsvärden direkt, men om din spektrofotometer bara ger dig resultatet av ljusintensitetsmätningen kan du beräkna dem själv.- För att hitta transmittansen (T), dela ljusintensiteten som gick genom provet med ljusintensiteten som gick genom det vita. Uttryck ditt resultat i procent eller i decimalform. T = I / I0, med I intensiteten uppmätt för lösningen och I0 intensiteten uppmätt för den vita.
- Absorbans (A) är den negativa för överföringsvärdets baslogaritm: A = -log10T. För ett värde av T lika med 0,1, kommer A att vara värt 1 (0,1 är lika med 10 effekt -1), vilket innebär att 10% av ljuset överförs och 90% absorberas. Med ett värde på T lika med 0,01, kommer A att vara värt 2 (eftersom 0,01 är lika med 10 effekt -2), vilket innebär att 1% av ljuset överförs.
-

Placera dina resultat på en graf. Värdet på absorbansen kommer att ligga på den vertikala axeln x, medan våglängden är på den horisontella axeln y. Det faktum att på en ortonormal ram har de maximala värdena på absorbansen för var och en av de testade våglängderna gör det möjligt att realisera absorptionsspektret för provet, identifiera närvarande föreningar och veta deras proportioner.- I allmänhet uppvisar absorptionsspektrum toppar vid vissa våglängder, vilket gör det möjligt att identifiera specifika föreningar.
-

Jämföra. Koppla ditt spektrum till de som är kända för olika kemiska föreningar. Varje ämne har ett eget absorptionsspektrum och kommer alltid att ha samma topp vid samma våglängd under mätningarna. Så du kan identifiera de okända föreningar som utgör din lösning genom att jämföra dess spektrum med graferna över kända föreningar.- Denna metod kan också vara användbar för att identifiera ämnen som skulle ha förorenat provet. Om det förväntade resultatet måste vara en topp vid en viss våglängd och du hamnar med två toppar vid två olika våglängder, beror det faktiskt på att det är något fel med din lösning.